Như những em đã biết trong phản bội ứng thoái hóa Khử, chất khử là hóa học nhường (cho) electron và hóa học oxi hóa là chất thu (nhận) electron. Đối cùng với phương trình thoái hóa khử, ta rất có thể cân bằng phương trình hóa học của bội nghịch ứng theo phương thức thăng bởi electron.
Vậy thăng bằng phương trình hóa học đối với phản ứng oxi hóa - Khử bằng phương thức thăng bởi electron dựa trên nguyên tắc nào? chúng ta cùng ôn lại trong bài viết này và giải những bài tập thăng bằng phương trình hóa học, bội phản ứng thoái hóa khử bằng cách thức thăng bằng electron để nắm rõ hơn câu chữ này.
I. Phương pháp thăng bởi electron
- Để thăng bằng phương trình phản nghịch ứng hóa học bằng phương pháp thăng bằng electron điều quan lại trọng bậc nhất là bọn họ phải khẳng định được số oxi hóa của những nguyên tố gia nhập phản ứng oxi hóa - khử. Dưới đấy là các quy tắc khẳng định số Oxi hóa của những nguyên tố thâm nhập phương trình làm phản ứng thoái hóa khử.
1. Quy tắc xác định số oxi hóa trong phản nghịch ứng oxi hóa khử.
● luật lệ 1: Số oxi hóa của những nguyên tố trong đối chọi chất bằng 0.
● Quy tắc 2: Trong đa số các vừa lòng chất :
- Số lão hóa của H là +1 (trừ các hợp chất của H với sắt kẽm kim loại như NaH, CaH2, thì H gồm số lão hóa –1).
- Số oxi hóa của O là –2 (trừ một vài trường phù hợp như H2O2, F2O, oxi bao gồm số oxi hóa thứu tự là : –1, +2).
● Quy tắc 3: Trong một phân tử, tổng đại số số oxi hóa của các nguyên tố bằng 0. Theo luật lệ này, ta rất có thể tìm được số lão hóa của một nguyên tố nào kia trong phân tử ví như biết số oxi hóa của các nguyên tố còn lại.
● luật lệ 4: Trong ion đơn nguyên tử, số lão hóa của nguyên tử bởi điện tích của ion đó. Vào ion đa nguyên tử, tổng đại số số oxi hóa của những nguyên tử trong ion đó bởi điện tích của nó.
> Chú ý:
- Để màn trình diễn số oxi hóa thì viết dấu trước, số sau, còn để trình diễn điện tích của ion thì viết số trước, dấu sau. Ví dụ: Số lão hóa Fe+3 còn ion sắt (III) ghi Fe3+.
- Nếu điện tích là 1+ (hoặc 1–) hoàn toàn có thể viết đơn giản là + (hoặc -) thì so với số oxi hóa phải viết tương đối đầy đủ cả dấu và chữ (+1 hoặc –1).
- Trong hợp chất, số oxi hóa của kim loại kiềm luôn là +1, kiềm thổ luôn luôn là +2 và nhôm luôn là +3.

2. Phương thức thăng bằng electron cân bằng phương trình phản bội ứng lão hóa khử
- Để lập phương trình phản ứng oxi hoá - khử theo cách thức thăng bằng electron, ta thực hiện công việc sau đây:
* ví dụ 1: Lập PTHH của phản bội ứng phường cháy vào O2 tạo thành P2O5 theo phương trình:
P + O2 → P2O5
• Bước 1: Xác định số oxi hoá của các nguyên tố trong bội phản ứng nhằm tìm hóa học oxi hoá và hóa học khử.
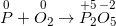
• Bước 2: Viết quy trình oxi hoá và quá trình khử, thăng bằng mỗi thừa trình.
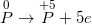
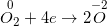
• Bước 3: Tìm hệ số tương thích cho chất oxi hoá và hóa học khử, làm sao để cho tổng số electron bởi chất khử nhường bởi tổng số electron mà hóa học oxi hoá nhận.
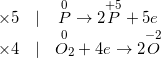
• Bước 4: Đặt các hệ số của hóa học oxi hoá và hóa học khử vào sơ vật phản ứng, tính các hệ số của những chất khác, đánh giá sự cân bằng của những nguyên tử của những nguyên tố ở hai vế,hoàn thành phương trình hoá học.
4P + 5O2 → 2P2O5
* ví dụ như 2: Lập PTHH của cacbon monooxit khử fe (III) oxit ở nhiệt độ cao, thành sắt cùng cacbon đioxit theo PTPƯ sau:
Fe2O3 + CO
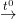
• Bước 1: Xác định số oxi hoá
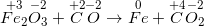
- Số oxi hoá của Fe bớt từ +3 xuống 0 ⇒ fe trong Fe2O3 là hóa học oxi hoá
- Số oxi hoá của C tăng tự +2 lên +4 ⇒ C trong CO là hóa học khử
• Bước 2: Viết quy trình oxi hoá và quá trình khử
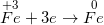
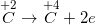
• cách 3: Tìm hệ số phù hợp cho hóa học oxi hoá và chất khử
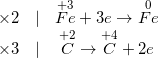
• Bước 4: Đặt các hệ số của chất oxi hoá và hóa học khử vào sơ đồ gia dụng phản ứng, ngừng PTHH.
Fe2O3 + 3CO → 2Fe + 3CO2
* lấy ví dụ 3: Cân bằng phương trình làm phản ứng thoái hóa khử:
a) fe + HNO3 → Fe(NO3)2 + NO + H2O
b) sắt + HNO3 → Fe(NO3)2 + NO2 + H2O
* hướng dẫn:
a) sắt + HNO3 → Fe(NO3)2 + NO + H2O
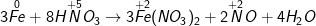
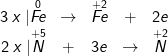
b) fe + HNO3 → Fe(NO3)2 + NO2 + H2O
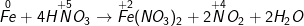
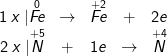
* lấy ví dụ như 4: Cân bởi phương trình phản bội ứng thoái hóa khử:
a) Zn + HNO3 → Zn(NO3)2 + NO + H2O
b) Zn + HNO3 → Zn(NO3)2 + NO2 + H2O
* phía dẫn:
a) Zn + HNO3 → Zn(NO3)2 + NO + H2O
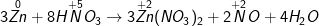
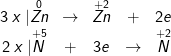
b) Zn + HNO3 → Zn(NO3)2 + NO2 + H2O
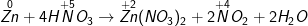
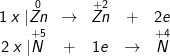
II. Bài xích tập cân đối phương trình phản nghịch ứng oxi hóa khử bằng phương pháp thăng bằng electron
> lưu ý: Với phản nghịch ứng lão hóa khử, đề xuất nhớ:
- Khử đến – O nhận
- thương hiệu của chất và tên quy trình ngược nhau
- hóa học khử là hóa học sẽ nhường electron (hay mang đến e) - đó quy trình oxi hóa.
- chất oxi hóa là chất mà thu electron (hay nhấn e) - kia là quy trình khử.
* bài bác 1(Bài 7 trang 83 sgk hóa 10): Lập phương trình làm phản ứng thoái hóa – khử dưới đây theo cách thức thăng bởi electron:
a) mang lại MnO2 tác dụng với dung dịch axit HCl đặc, thu được MnCl2, Cl2 và H2O.
b) cho Cu tính năng với hỗn hợp axit HNO3 đặc, lạnh thu được Cu(NO3)2, NO2, H2O.












