Bảng tính chảy hoá học là phần không thể thiếu trong bộ môn hóa học lớp 8, 9, 10, 11. Chúng bao gồm những kiến thức về hóa học kết tủa, chất cất cánh hơi, chất không chảy trong nước... Mặc dù với nhiều tin tức như vậy sẽ tương đối khó trong phần ghi lưu giữ đối với chúng ta học sinh. Bài viết dưới đây sẽ giúp đỡ bạn nuốm chắc kỹ năng và kiến thức và biện pháp học thuộc bảng tính tan dễ nhất nhé.
Nội dung chính Các yếu tố tác động đến độ tung của một chấtCách học thuộc nhanh bảng tính tan nhanh nhất
1. Định nghĩa về độ hòa tan
Độ hòa tan xuất xắc độ tan cho biết khả năng tổ hợp của một chất ( rắn, lỏng, khí ) vào dung môi để tạo thành một hóa học bão hòa trong nhiệt độ nước.
Với đặc trưng ở trên có thể xác định được chất tan hay là không tan nhờ vào thông tin sau:
Nếu lấy trên 10g hóa học đó có thể hòa rã được vào 100g nước hòa tan thì chất này được call là chất tan hay hóa học dễ tanNếu chỉ bên dưới 1g chất này được hòa rã trong 100g nước thì kia là chất ít tanNếu chỉ tất cả 0,01 chất đó được hòa tan trong 100g nước thì chúng được gọi là hóa học không tan2. Bảng tính chảy hóa học không hề thiếu của Muối, Axit với Bazo
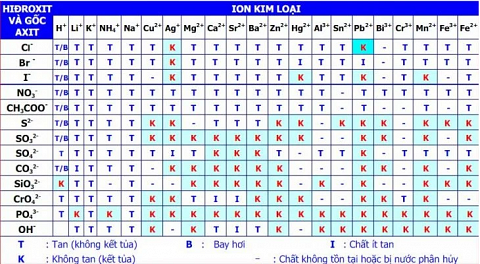
| HIDROXIT cùng GỐC AXIT | ION KIM LOẠI | ||||||||||||||||||||
| H+ | Li+ | K+ | NH4+ | Na+ | Cu2+ | Ag+ | Mg2+ | Ca2+ | Sr2+ | Ba2+ | Zn2+ | Hg2+ | Al3+ | Sn2+ | Pb2+ | Bi3+ | Cr3+ | Mn2+ | Fe3+ | Fe2+ | |
| Cl- | T/B | T | T | T | T | T | K | T | T | T | T | T | T | T | T | K | - | T | T | T | T |
| Br- | T/B | T | T | T | T | T | K | T | T | T | T | T | I | T | T | I | - | T | T | T | T |
| I- | T/B | T | T | T | T | - | K | T | T | T | T | T | K | T | T | K | - | T | K | - | T |
| NO3- | T/B | T | T | T | T | T | T | T | T | T | T | T | T | T | - | T | T | T | T | T | T |
| CH3COO- | T/B | T | T | T | T | T | T | T | T | T | T | T | T | T | - | T | - | - | T | - | T |
| S2- | T/B | T | T | T | T | K | K | - | T | T | T | K | K | - | K | K | K | - | K | K | K |
| SO32- | T/B | T | T | T | T | K | K | K | K | K | K | K | K | - | - | K | K | - | K | - | K |
| SO42- | T | T | T | T | T | T | I | T | K | K | K | T | - | T | T | K | - | T | T | T | T |
| CO32- | T/B | T | T | T | T | - | K | K | K | K | K | K | - | - | - | K | K | - | K | - | K |
| SiO32- | K | T | T | T | T | - | - | K | K | K | K | K | - | K | - | K | - | - | K | K | K |
| CrO42- | T | T | T | T | T | K | K | T | I | I | K | K | K | - | - | K | K | T | K | - | - |
| PO43- | T | K | T | K | T | K | K | K | K | K | K | K | K | K | K | K | K | K | K | K | K |
| OH- | T | T | T | T | K | - | K | T | I | T | K | - | K | K | K | K | K | K | K | K |
Giải phù hợp bảng tính tan:
I : hóa học Ít tan
K : ko tan ( Kết tủa )
T : chảy ( không kết tủa )
- : chất không trường tồn hoặc bị nước phân hủy
B : cất cánh hơi
Để giải những vấn đề hóa học về tính chất tan, kết tủa hay sự cất cánh hơi trong phòng phân tách thì học sinh cần phải có được phiếu tính tan. Vì vậy, những kiến thức và kỹ năng trong bảng tính rã đầy đủ thì bạn cần phải nắm rõ.
Bảng tính tan hóa học bao gồm rất nhiều kỹ năng và cả hầu hết quy tắc vì thế mà bài toán ghi nhớ kiến thức này không còn dễ dàng. Theo đó chúng ta hãy tra cứu cụ thể thông tin trong các số đó để dữ thế chủ động giải và cách xử lý những bài toán về hóa học xuất xắc khi làm các thí nghiệm.
3. Các yếu tố tác động đến độ tan của một chất
Tính hóa chảy của một chất bao gồm tác động của tương đối nhiều yếu tố, vì thế các bạn phải nắm được tin tức sau đây:
3.1. Sức nóng độ
Đối với hóa học khí, độ tan của nó sẽ tỷ lệ nghịch với ánh sáng khi trong dung môi. Người ta hay đun nóng hóa học khí để sa thải những hóa học như CO2 với O2 thoát ra khỏi dung môi nhưng mà không làm đổi khác cũng như làm cho phân hủy chất. Đồng thời còn hỗ trợ được dược hóa học ổn định.Chất rắn thu nhiệt thì lúc nhiệt độ càng cao khiến đến độ hòa hợp càng lớn. Còn với hóa học rắn tỏa sức nóng khi kết hợp thì trái lại nhiệt độ càng giảm, độ tan đã càng tăng.3.2. Áp suất (đối với chất khí)
Như chúng ta học hóa đã biệt, trong định nguyên tắc Henry, nếu các chất khí tất cả độ tan nhỏ dại và áp suất không thật cao thì khi tăng áp suất trên mặt phẳng chất lỏng không đổi thì lượng hóa học khí hòa tan trong một thể tích chất lỏng xác định cũng trở thành tăng. Cùng ngược lại.3.3. Độ phân cực của hóa học tan cùng dung môi
Các hóa học phân cực cũng thường dễ tan rộng trong môi trường xung quanh dung môi phân cực rõ ràng như kiềm, nước, dung dịch muối tốt axit vô cơ,…Những hóa học ít phân cực cũng trở thành dễ tan môi trường dung môi hữu cơ yếu phân cực bao hàm chloroform, benzene, toluene, dicloromethan,…3.4. Dạng thù hình
Thường một số loại chất rắn dạng vô định hình sẽ có độ tan lớn hơn so với chất rắn dạng tinh thể trong thuộc một môi trường thiên nhiên dung môi. Đó là vì chưng khi chất rắn sinh sống dạng kết tinh thì đã có cấu trúc mạng lưới tinh thể tương đối bền vững. Thế cho nên mà nó nên nhiều năng lượng để rất có thể phá vỡ cấu trúc hơn. Trái lại thì chất rắn dưới dạng vô đánh giá sẽ tạm thời như dạng tinh thể, chúng có xu thế chuyển sang trọng dạng tinh thể.3.5. Hiện tượng kỳ lạ hydrat hóa
Trong quá trình kết tinh, chất rắn thường rất có thể được tồn tại dưới dạng ngậm nước hoặc dạng khan. Đối với dạng ngậm nước, hóa học rắn ở dạng khan sẽ có tính tan lớn hơn.3.6. Hiện tượng kỳ lạ đa hình
Với môi trường xung quanh kết tinh khác nhau sẽ tạo đk để hóa học rắn mãi sau dưới những dạng tinh thể khác nhau bao hàm Hydrat, đồng kết tinh, .. Với những đặc điểm vật lý cùng độ chảy trong dung môi rất khác nhau. Hay với phần nhiều tinh thể kém chắc chắn thì sẽ yên cầu ít tích điện trong phá vỡ cấu tạo do vậy cơ mà dễ chảy hơn.3.7. Độ pH của dung dịch
Khi kiềm hóa dung môi, axit yếu sẽ có được độ tung tăng lênNếu axit hóa dung môi, độ tan của các chất kiềm yếu đã tăng lênĐối với phần lớn chất lưỡng tính, độ tan của các chất này sút dần khi mà lại độ pH càng sát điểm đẳng điện với ngược lại.3.8. Hóa học điện ly
Độ tan của những chất tan hoàn toàn có thể bị sút trong chất điện ly vào dung dịch bởi vì vậy bạn cần phải lưu ý trộn loãng chất điện ly trước khi hòa vào dung dịch.
3.9. Những ion cùng tên
Trường đúng theo nồng độ của các ion thuộc tên tăng lên, có thể làm cân bằng điện ly của chất tan thì vẫn làm đưa dịch về hướng phân tử không nhiều tan cùng làm giảm sút độ rã của chất. Vì vậy mà trong quá trình hóa tan, bạn phải tiến hành với đầy đủ chất không nhiều tan trước, kế tiếp mới tới những chất dễ tan.
3.10. Hỗn hợp dung môi
Nếu như bạn phối hợp các các thành phần hỗn hợp dung môi đồng tan cùng với nước ví dụ như glycerin-ethanol-nước thì sẽ làm tăng cường độ tan của những chất khó khăn tan.
3. Giải pháp đọc bảng tính tan dễ dàng
Bảng tính tan hóa học lớp 9 bao gồm các cột và những hàng các chúng ta có thể tìm hiểu dễ ợt trong sách giáo khoa. Trong đó, cách gọi bảng tính tan là theo hàng gồm anion cội axit (OH-) còn cột là các cation kim loại. Trong đó có một số trong những chất cố thể, fan ta rất có thể xác định được ion âm cùng ion dương, chúng được xếp theo hàng với cột tương ứng khiến cho bạn nắm được tâm lý của hóa học đó.
4. Bí quyết học thuộc cấp tốc bảng tính tan nhanh nhất
Đối với các môn kỹ thuật như chất hóa học thì điều đặc biệt quan trọng đó là các bạn cần phải luyện tập và làm cho nhiều bài bác tập nhằm rèn luyện về tính ghi nhớ tương tự như điều kiện hòa tan của các hợp chất. Như vậy sẽ giúp cho chúng ta tìm hiểu sâu hơn về thực chất của các phản ứng hóa học, đồng thời dễ dàng ghi ghi nhớ tính tan đối với những hóa học thường chạm mặt trong bảng tính tan.
Mặc mặc dù thế thì việc ghi nhớ tổng thể bảng tính tan tan cũng sẽ chạm mặt nhiều trở ngại và dễ dẫn đến nhầm lẫn. Các bạn chuyên hóa thường truyền tai nhau phần nhiều mẹo với cách học tập bảng tính tan cấp tốc nhất và tác dụng nhé:
4.1. Thực hành thực tế thường xuyên
Một trong số những cách học tập bảng tính rã lớp 9 cùng lớp 11 sớm nhất có thể đó chính là phải thực hành lặp đi lặp lại. Nếu khách hàng được học trong môi trường tốt thì sẽ sở hữu điều khiếu nại được liên tục thực hành môn hóa học sẽ khá tốt. Điều cốt lõi so với môn hóa học đó là chúng ta phải nạm được thực chất của các phản ứng hóa học. Điều này được biểu lộ rõ hơn khi chúng ta tận mắt bệnh kiến những điều kiện, làm phản ứng xẩy ra nếu làm trong chống thí nghiệm.
Đồng thời các bạn cần phải kết phù hợp với việc làm nhiều bài tập về nhà, việc thực hành nhiều sẽ giúp bạn nắm được đặc thù tan của một vài chất thường xuyên dùng. Các bạn sẽ dần quen thuộc với bảng tính tan các muối hay của các chất khác cùng dễ nhớ hơn hơn thỉnh thoảng được lặp lại thường xuyên.
Những kiến thức và kỹ năng hóa học tập thường gặp nhiều trong công tác THPT, đấy là nền tảng nhằm bạn áp dụng vào cuộc sống. Tuyệt nhất là cùng với những bạn học tại các trường Đại học, Cao đẳng Y Dược HCM thì vận dụng nhiều trong quy trình học và sau khoản thời gian đi làm. Nó sẽ giúp bạn đảm nhiệm tốt các công việc chuyên môn cùng có thời cơ thăng tiến vào cuộc sống.
4.2. Cách ghi nhớ bảng tính tan bởi hình ảnh

Bảng tính tan gồm 1 lượng kỹ năng và kiến thức không nhỏ và chúng rất dễ tạo nhầm lẫn với nhau. Đây cũng là phần nhiều kiến thức căn cơ của môn hóa học., vì vậy các bạn phải có phương pháp và cách biểu hiện học tập chuyên tâm. Trường hợp chỉ học vẹt, học tập một bí quyết vô thức thì chỉ ghi lưu giữ được gần như thứ trước mắt, rất đơn giản quên nếu như không thường xuyên vận dụng. Trong những cách học bảng tính tan của những chất đó là thông qua hình ảnh.
Đây là phương pháp học không hề mới lạ được áp dụng trong tương đối nhiều bộ môn không giống nhau, điển hình là ghi nhớ. Nhiều minh chứng cho thấy, mắt có tác động ảnh hưởng lớn cho tới não cỗ với kĩ năng ghi nhớ của bé người. Vì vậy mà thông qua hình ảnh cũng là biện pháp giúp cho bạn ghi nhớ bảng tính tan những chất.
4.3. Học thuộc những quy tắc rút gọn về tính chất tan
Độ rã của muối, axit, bazo nội địa vừa được share ở trên, bạn cũng có thể ghi ghi nhớ tính tan của các chất này vào nước. Ví dụ như:
4.3.1. Đối với muối:Các muối bao gồm gốc halogen như -Br, -Cl, -F… thì đều có chức năng tan vào nước.Muối cội Sunfit (SO3), Silicat (SiO3), Cacbonat (CO3) hay Sunfua (S) những sẽ cực nhọc tan, thậm chí là không chảy trong nước. Mặc dù nhiên, nếu những gốc này kết hợp với kim loại có tính kiềm thì chúng sẽ tạo ra đa số hợp hóa học muối tung được vào nước.Ngoài ra, một trong những kim loại kiềm bao hàm Na, K, Li… sau khi kết hợp thành muối thì bọn chúng đều hoàn toàn có thể tan trong nước. Nhìn vào bảng tính tung hóa hoàn toàn có thể thấy những hàng tất cả chứa kim loại tính kiềm, ký hiệu bằng văn bản T, có nghĩa là các hóa học dễ tan.Muối gốc Sunfat (SO4) nhiều phần đều tan trong nước, trừ muối bột sunfat của sắt kẽm kim loại bari không tan.Lưu ý: một số trong những muối không tồn tại hoặc chúng có thể bị phân huỷ tức thì trong nước thì vào bảng tính rã được cam kết hiệu bởi dấu “-“. Những trường hòa hợp này rất ít nhưng cũng gần buộc phải ghi ghi nhớ nhé.
4.3.2. Đối với axit cùng bazo:Mọi các loại axit những tan thuận tiện trong nước, tuy vậy có H2CO3 đang dễ bị phân huỷ trong nước và các axit có gốc silicic như H2SiO3, H4SiO4… thì ko tan.Các bazo thì đa số không tan trong nước, quanh đó bazo của kim loại kiềm như Li, K, N phần đa tan vào nước cùng bazo của kim loại nhóm 2 sẽ ít chảy trong nước.4.4. Học thuộc bảng tính rã qua thơ
4.4.1. Bài xích thơ Tính tan của muốiLoại muối bột tan tất cả
là muối hạt ni tơ rat
Và muối bột a xê tat
Bất kể sắt kẽm kim loại nào
Những muối phần đông tan
Là clorua, sunfat
Trừ bạc đãi chì clorua
Bari, chì sunfat
Những muối không hoà tan
Cacbonat, photphat
Sunfua với sunfit
Trừ kiềm, amoni.
4.4.2 bài thơ tính tan của các chất hóa họcBazơ, đông đảo chú không tan:
Đồng, nhôm, crôm, kẽm, mangan, sắt, chì.
Ít tung là của Canxi
Magiê cũng chẳng điện ly dễ dàng
Muối sắt kẽm kim loại I đầy đủ tan
Cũng như Nitrat với “nàng” hữu cơ
Muốn ghi nhớ thì cần làm thơ!
Ta làm thì nghiệm bây giờ thử coi,
Kim nhiều loại I, ta biết rồi,
Những sắt kẽm kim loại khác ta “moi” ra tìm
Photphat vào nước “đứng im” (Trừ kim loại I)
Sunphat một số trong những “im lìm trơ trơ”:
Bari, chì cùng với S – r
Ít tan bao gồm bạc, “chàng khờ” Canxi,
Còn muối hạt Clo – rua thì bạc đãi đành kết tủa, anh chì cầm tan (Giống muối hạt Br, I)
Muối khác thì nhớ dễ dàng:
Gốc S O 3 chẳng chảy chút nào! (Trừ kim loại I)
Thế còn cội S thì sao? (Giống muối hạt cacbonat)
Nhôm ko tồn tại chú nào thì cũng tan
Trừ đồng, thiếc, bội bạc mangan,
Thủy ngân, kẽm, sắt không tan cùng chì
Đến trên đây thì đã đủ thi,
Thôi thì chúc bạn trường gì rồi cũng vô!
Với kỹ năng và kiến thức về bảng tính tan trên đây mong muốn sẽ là hành trang giúp các bạn học tập giỏi môn Hóa. Nếu yêu thích, yêu thích ngành Y Dược thì đừng bỏ qua trường cđ Y Khoa Phạm Ngọc Thạch nhé.












